Bei der Elektrolyse sind die elektrischen Leitungsvorgänge mit einer Stoffabscheidung verbunden. Die abgeschiedene Stoffmenge ist proportional zur transportierten Ladung Q, die den Elektrolyten durchflossen hat. Bei diesem Zusammenhang handelt es sich um das Faraday'sche Gesetz.
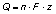
z = Ladungszahl des verwendeten Ions
F = Faraday-Konstante
Im Versuch C4.4.5.2 wird die Faraday-Konstante F bestimmt. Dafür wird eine bestimmte Menge Wasserstoff mit einem Hofmannschen Zersetzungsapparat erzeugt. Die Molzahl n der abgeschiedenen Wasserstoffatome berechnet man mit Hilfe der Idealen Gasgleichung aus dem Volumen V. Gleichzeitig wird die dafür benötigte Ladungsmenge Q über die elektrische Arbeit W bestimmt.
Der Versuch kann als CPS-Version oder mit Stativmaterial aufgebaut werden.
